Химия: Химическая реакция
Версия от 13:12, 7 марта 2018; Admine2 (обсуждение | вклад)
Превращение одних веществ в другие называется химической реакцией. Исходные вещества, которые вступают в химическую реакцию называются реагентами, а новые вещества, которые образуются в результате химической реакции называются продуктами реакции.
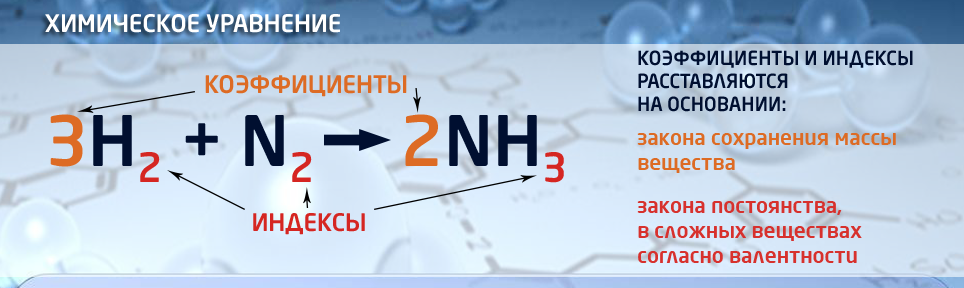
- Химическое уравнение – это выражение химической реакции с помощью химических формул веществ, изображенных условными знаками. В химическом уравнении, изображенным с помощью химических формул, различают левую и правую части уравнения. В левой части указывают реагенты, в правой части - продукты реакции. В формулах веществ индексами показывают количество атомов химического элемента, входящих в состав данного вещества. Это существенно влияет на свойства веществ:
-
H2SO4 H2SO3 Серная кислота Сернистая кислота Сильная Слабая Устойчивая Нестойкая Наносит сильные ожоги На свету разлагается Маслянистая жидкость Водный раствор газа
В химических уравнениях перед формулами записывают коэффициенты, которые показывают количество молекул, принимающих участие в химической реакции.
Обычно в химическом уравнении равенство ставят тогда, когда указывают количество выделенной или поглощенной энергии. (Это тепловой эффект реакции) 2Mg + O2 = 2MgO + 1203 кДж. При написании химических уравнений используют стрелку, показывающую направление реакции: SO2 + H2O ![]() H2SO3
H2SO3
Содержание
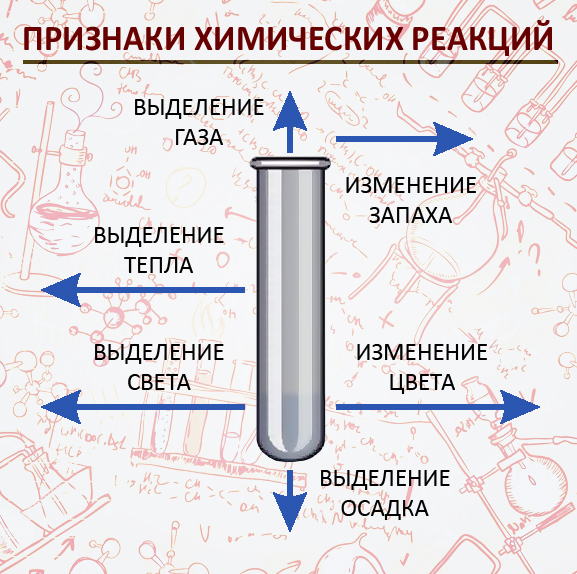
Признаки химических реакций
- Выделение тепла
Опыт № 54 или (горение костра) - Выделение света
Опыт № 3 (горение серы в кислороде) - Образование осадка
Опыт № 77 (галогены с ионом серебра) - Выделение газа
Опыт № 37 (медь с конц. азотной кислотой –«лисий хвост») - Изменение цвета
Опыт № 75 (хлорид кобальта с гидроксидом натрия – синий цвет) - Изменение запаха
(гниющий мусор)
Изменения, происходящие с веществами, свидетельствуют о протекании химических реакций и являются признаками химических реакций.
Большинство веществ не могут взаимодействовать друг с другом самопроизвольно. Для протекания многих химических реакций необходимо создавать определенные условия.
Условия, необходимые для начала химической реакции

- 1. Измельчить 2. Перемешать 3. Нагреть
Для обеспечения лучшего контакта вещества измельчают, переводят в газообразное состояние. Многие вещества лучше реагируют друг с другом, если они растворены в воде.
Во многих случаях этого недостаточно, поэтому реагирующие вещества нагревают. Деревянная лучинка, смесь железа и серы, медь могут долгое время сохраняться при комнатной температуре, реакции начинаются только при их нагревании.
В некоторых случаях для начала химического процесса необходимо освещение. Одной из таких реакций, требующих постоянного освещения, является известная вам реакция фотосинтеза.
Классификация химических реакций
Таблица
Реакцией соединения называется реакция, в результате которой из двух или нескольких веществ образуется одно новое вещество. S + O2 SO2 CaO + H2O Ca(OH)2 CaCO3 + CO2 + H2O Ca(HCO3)2
Реакцией разложения называется реакция, в результате которой из одного вещества образуется два или нескольких новых веществ. 2HgO 2Hg + O2 Сu(OH)2 СuO +H2O 2AgNO3 2Ag + 2NO2 + O2
Реакцией замещения называется реакция между простым и сложным веществом, при которой атомы простого вещества замещают атомы в сложном веществе по принципу: в новом веществе атомы с наибольшей электроотрицательностью соединяются с атомами с наименьшей электроотрицательностью. Атомы элемента с промежуточной между ними электроотрицательностью высвобождаются в виде простого вещества. В результате образуются новое сложное и новое простое вещества. Fe + CuSO4 FeSO4 + Cu 1,56 1,75 1,56 1,75 Zn + 2HCl ZnCl2 + H2 1,66 2,1 1,66 2,1 2KBr + Cl2 2KCl + Br2
2,7 3,0 3,0 2,7
Реакцией обмена называется реакция между двумя сложными веществами при которой они обмениваются своими составными частями. Причем та часть, что стояла первой, в новом веществе будет стоять первой, а та часть, что стояла второй и в новом веществе тоже будет стоять на втором месте. AgNO3 + NaCl AgCl↓ + NaNO3 NaOH + HCl NaCl + H2O FeCl3 + 3NaOH Fe(OH)3↓ +3NaCl
Экзотермическими реакциями называются реакции, идущие с выделением теплоты. Многие реакции соединения являются экзотермическими реакциями.
Эндотермическими реакциями называются такие реакции, которые идут с поглощением теплоты Эндотермическими реакциями являются многие реакции разложения.
Количество теплоты, которое выделяется или поглощается при химический реакции, называется тепловым эффектом реакции.
Каталитическими реакциями называются такие реакции, которые идут только в присутствии катализатора. Использование различных катализаторов приводит к получению различных продуктов реакции.
Катализаторами называют вещества, которые влияют на скорость реакции, чаще всего, ускоряя скорость реакции.
Катализаторы принимают непосредственное участие в химической реакции, но по окончании реакции высвобождаются.
Катализаторы, замедляющие скорость химических реакций называются ингибиторами.
Химические реакции, которые идут без участия катализаторов называются некаталитическими.
Окислительно–восстановительными реакциями являются такие реакции, в которых у атомов, входящих в состав молекул, изменяются степени окисления по окончании реакции.
Окислительно–восстановительными чаще бывают реакции соединения и обмена.
Бывают реакции, которые протекают без изменения степеней окисления элементов
У необратимых реакций только одна скорость и они протекают только в одну сторону, если продуктом реакции является осадок, газообразное вещество или вода.
Реакции, приводящие к установлению химического равновесия, называются обратимые. У обратимых реакций две скорости – скорость прямой реакции, приводящая к образованию продукта реакции. И скорость обратной реакции – распад продукта реакции до исходных веществ. Когда скорости прямой и обратной реакций становятся равными, наступает химическое динамическое равновесие. Это означает, что в единицу времени образуется столько молекул, сколько их распадается за это же время.
Гомогенными называются реакции, в которых все реагирующие вещества, продукты реакции и катализатор тоже в каталитических реакциях, находятся в одном агрегатном состоянии. Если хотя бы одно из веществ имеет другое агрегатное состояние, то такая реакция называется гетерогенной. ( Гомо – одинаковый, гетеро – разный).
Образование разных простых веществ одним элементом называется аллотропией. Аллотропия возникает или из–за разного количества атомов в составе вещества (O2 –кислород, O3 – озон), или из–за разного соединения атомов в кристаллическую решетку (алмаз, графит).
Изомеры – это вещества одинакового качественного и количественного состава, но разное строение молекул и различные свойства.
Глассарий
- Анионы - отрицательно заряженные ионы.
Полезные ссылки
Бибилиография
нету
- Ахметов Н. С. Актуальные вопроса курса неорганической химии. — М.: Просвещение, 1991. — 224 с — ISBN 5-09-002630-0