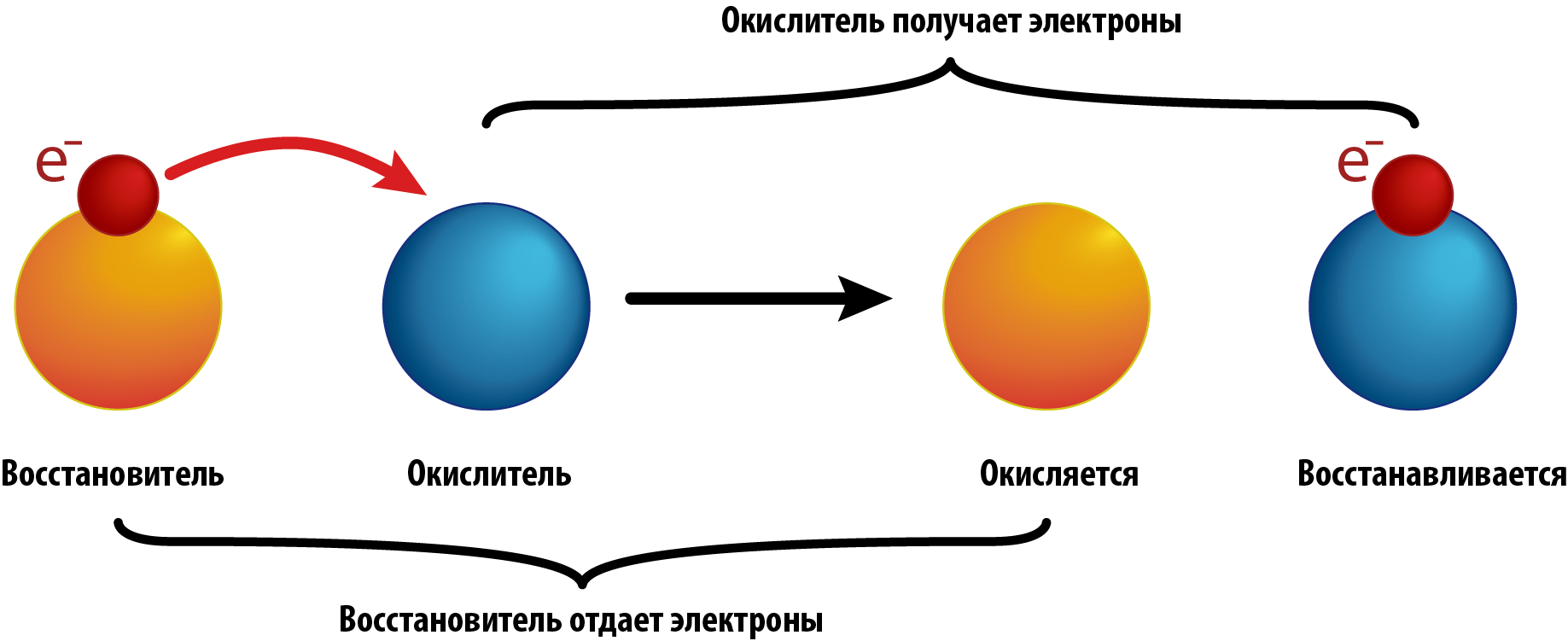Химия: Окислительно-восстановительные реакции
Окислительно-восстановительными реакциями являются такие реакции, в которых у атомов, входящих в состав молекул изменяются степени окисления по окончании реакции.
Отдельно не существует процесса окисления или процесса восстановления. Есть процесс передачи электронов от атомов одного элемента к атомам другого элемента. В реакциях самоокисления – самовосстановления участвуют атомы одного элемента, только часть из них отдает электроны, а другая часть их принимает.
Окислители всегда имеют наибольшее значение электроотрицательности. В формулах сложных веществ всегда есть как окислители, так и восстановители. Окислитель в формуле вещества всегда один – это атом с наибольшей электроотрицательностью, он заряжен отрицательно.
Восстановителей в формуле сложного вещества может быть 1, 2, 3, они все имеют положительный заряд. В формуле вещества количество отрицательных зарядов на атомах окислителя равно сумме положительных зарядов на атомах всех восстановителей. В целом атом - электронейтральная частица. На этом балансе электронов основано решение окислительно-восстановительных уравнений.
Содержание
Классификация ОВР
Решение межмолекулярных ОВР
В классических вариантах окислительно-восстановительных реакций всегда есть три действующих компонента:
вещество, на которое направлен процесс,
вещество окислитель
вещество - подкислитель (чаще всего эти реакции идут в кислой среде) – обычно оно богато главным и самым распространенным окислителем – кислородом.
5H2S + 2KMnO4 + 3H2SO4![]() K2SO4 + 2MnSO4 + 5S↓ + 8H2O
K2SO4 + 2MnSO4 + 5S↓ + 8H2O
В данном уравнении:
H2S – вещество, на которое направлен процесс,
KMnO4 – вещество окислитель
H2SO4 – вещество – подкислитель.
1. Определить степени окисления атомов в формулах всех веществ:
H2S + KMnO4 + H2SO4![]() K2SO4 + MnSO4 + S↓ + H2O
K2SO4 + MnSO4 + S↓ + H2O
2. Подчеркнуть элементы, изменившие степени окисления до реакции и после реакции:
H2S + KMnO4 + H2SO4![]() K2SO4 + MnSO4 + S↓ + H2O
K2SO4 + MnSO4 + S↓ + H2O
3. В уравнение электронного баланса выписать данные с указанием степеней окисления до и после реакции:
Mn +7 -5e ![]() Mn 2+ | 5 | 2
Mn 2+ | 5 | 2
S +2 +2e ![]() S 0 | 2 | 5
S 0 | 2 | 5
Уравнение электронного баланса
4. В уравнение переносим коэффициенты, полученные в электронном балансе, 2 к Mn, 5 к S в правой стороне уравнения:
H2S + KMnO4 + H2SO4![]() K2SO4 + 2MnSO4 + 5S↓ + H2O
K2SO4 + 2MnSO4 + 5S↓ + H2O
Проставим эти же коэффициенты в левую часть уравнения
5H2S + 2KMnO4 + H2SO4![]() K2SO4 + 2MnSO4 + 5S↓ + H2O
K2SO4 + 2MnSO4 + 5S↓ + H2O
5. Уравниваем металлы. Калия по два атома слева и справа, следовательно у формулы K2SO4 стоит коэффициент 1.
5H2S + 2KMnO4 + H2SO4![]() 1K2SO4 + 2MnSO4 + 5S↓ + H2O
1K2SO4 + 2MnSO4 + 5S↓ + H2O
6. Уравниваем неметаллы. В правой части уравнения у всех веществ, содержащих серу, стоят коэффициенты. Сумма атомов серы равна 8. В левой части уравнения у сероводорода коэффициент равен 5, следовательно, надо добавить 3 серы, которая есть в серной кислоте. Ставим коэффициент 3 к молекуле серной кислоты.
5H2S + 2KMnO4 + 3H2SO4![]() 1K2SO4 + 2MnSO4 + 5S↓ + 8H2O
1K2SO4 + 2MnSO4 + 5S↓ + 8H2O
7.Считаем количество атомов водорода в левой части уравнения. У сероводорода 10 атомов и в серной кислоте 6 атомов. В сумме 16 атомов водорода. В правой части уравнения водород только в воде. В составе воды два водорода. Чтобы его количество соответствовало 16, делим на 2 и ставим к воде коэффициент равный 8..
8. Проверяем количество атомов кислорода в левой и правой частях уравнения:
2 • 4 + 3 • 4 = 4 + 2 • 4 + 8 | 20 = 20
9. Если количество атомов кислорода в левой части уравнения равно количеству атомов кислорода в правой части уравнения, решение правильное.
В межмолекулярных уравнениях бывает в левой части уравнения только два «действующих лица» и тогда происходит «совмещение функций». В этом уравнении азотная кислота и окислитель и подкислитель.
3Cu + 8HNO3(разб) ![]() 3Cu(NO3)2 + 2NO + 4H2O
3Cu(NO3)2 + 2NO + 4H2O
В уравнении 2KMnO4 +16HCl ![]() 5Cl2↑ + 2MnCl2 + 2KCl + 8H2O молекулы хлороводородной кислоты и окисляются до хлора в количестве 10 и являются подкислителями – 6.
5Cl2↑ + 2MnCl2 + 2KCl + 8H2O молекулы хлороводородной кислоты и окисляются до хлора в количестве 10 и являются подкислителями – 6.
Внутримолекулярные ОВР
Чаще всего это реакции разложения, идущие при нагревании.
2KMnO4 ![]() K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
4KMnO4 ![]() 2K2O + 4MnO2 + 3O2↑ (При очень высокой температуре)
2K2O + 4MnO2 + 3O2↑ (При очень высокой температуре)
2KClO3 ![]() 2KCl + 3O2↑
2KCl + 3O2↑
2NaNO3 ![]() 2NaNO2 + O2↑
2NaNO2 + O2↑
2HgO ![]() 2Hg +O2↑
2Hg +O2↑
2H2O2 MnO2→ 2H2O + O2↑
Среди реакций самоокисления – самовосстановления много интересных:
4KClO3 ![]() 3KClO4 + KCl
3KClO4 + KCl
3So + 6NaOH ![]() 2Na2S-2 +Na2S+4O3 + 3H2O
2Na2S-2 +Na2S+4O3 + 3H2O
Уравнение электронного баланса
Sо +2e → S-2 | 2 | 1 | 2
Sо -4e → S+4 | 4 | 2 | 1
2Н2S + H2SO3 ![]() 3S↓ + 3H2O
3S↓ + 3H2O
SO2 + 2H2S ![]() 3S↓ + 2H2O
3S↓ + 2H2O
Особое место среди ОВР занимает реакция использования черного пороха, где степени окисления изменяют сразу три элемента:
3C + S + 2KNO3 ![]() K2S + 3CO2↑ + N2↑
K2S + 3CO2↑ + N2↑
Уравнение электронного баланса
Sо +2e → S-2 | +2 | 4 | 1
Со -4e → С+4 | -4 | 12 | 3
2N+5 -10e → N2 0 | +10 | 4 | 1
В этом уравнении окислителей два – азот и сера, поэтому их электроны суммируются, а далее, сократившись, цифра ставятся к углероду. После сокращения коэффициент углерода 1 ставится к двум элементам - сере и азоту. Затем коэффициенты переносятся в уравнение реакции.
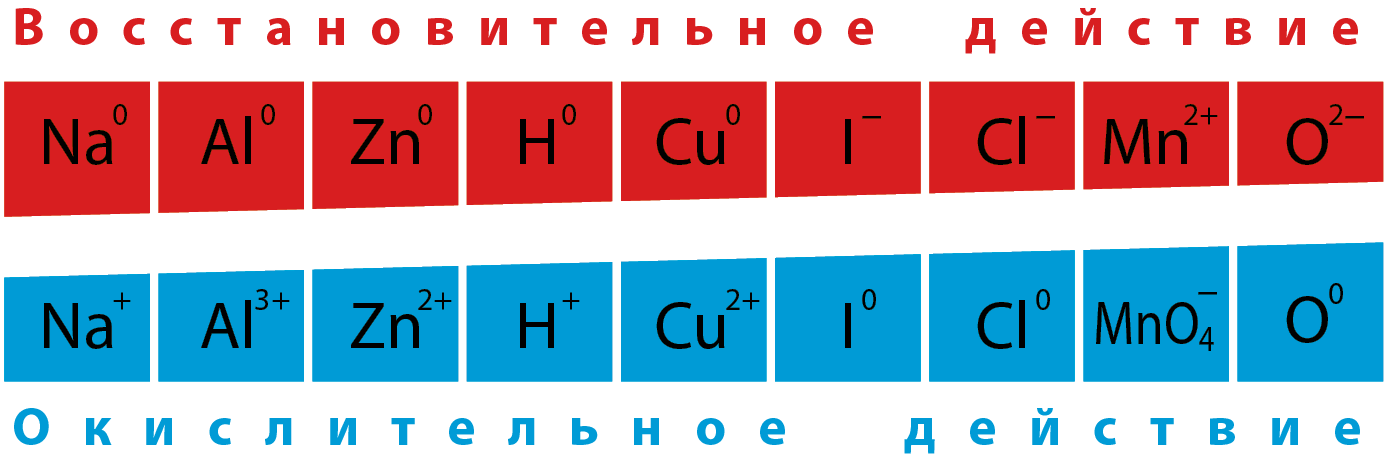
Окислителями могут быть вещества, в составе которых элементы, изменяющие степени окисления, находятся в высшей степени окисления:
(N +5) HNO3; (Mn +7) KMnO4, HMnO4; (Cr +6) K2CrO7. CrO3 ; (Pb +4) PbO2; (F 0 ) F2; (S +6) H2SO4.
Восстановителями могут быть вещества, в составе которых элементы, изменяющие степени окисления, находятся в низшей степени окисления:
(N -3) NH3; (S -2)H2S; (F. Cl, Br. I -1) HF. HCl, HBr. HI ; (P -3) РH3; ) Р -1) гидриды металлов; (все металлы в виде простого вещества) Na, Al, Mg….
Окислителями и восстановителями могут быть вещества, в составе которых элементы, изменяющие степени окисления, находятся в промежуточной степени окисления
(N =0 +3): N2, HNO2; (S=0) S; (Fe +2): FeSO4, FeCl2.
Расставьте коэффициенты в окислительно–восстановительных реакциях методом электронного баланса.
Zn + H2SO4(очень разбав) ![]() ZnSO4 + H2S↑ + H2O
ZnSO4 + H2S↑ + H2O
4Zn + 5H2SO4(очень разбав) ![]() 4ZnSO4 + H2S↑ + 4H2O
4ZnSO4 + H2S↑ + 4H2O
Cu + HNO3(разбав) ![]() Cu(NO3)2 + NO↑ + H2O
Cu(NO3)2 + NO↑ + H2O
3Cu + 8HNO3(разбав) ![]() 3Cu(NO3)2 + 2NO↑ + 4H2O
3Cu(NO3)2 + 2NO↑ + 4H2O
KI + MnO2 + H2SO4 ![]() K2SO4 + MnI2 + I2 + H2O
K2SO4 + MnI2 + I2 + H2O
4KI + MnO2 + 2H2SO4 ![]() 2K2SO4 + MnI2 + I2 + 2H2O
2K2SO4 + MnI2 + I2 + 2H2O
HCl + MnO2 ![]() Cl2↑ + MnCl2 + H2O
Cl2↑ + MnCl2 + H2O
4HCl + MnO2 ![]() Cl2↑ + MnCl2 + 2H2O
Cl2↑ + MnCl2 + 2H2O
S + HNO3(конц) ![]() H2SO4 + NO2 + H2O
H2SO4 + NO2 + H2O
S + 6HNO3(конц) ![]() H2SO4 + 6NO2 + 2H2O
H2SO4 + 6NO2 + 2H2O
Усложненные
FeCl2 + KMnO4 + HCl ![]() FeCl3 + MnCl2 + KCl + H2O
FeCl3 + MnCl2 + KCl + H2O
5FeCl2 + KMnO4 + 8HCl ![]() 5FeCl3 + MnCl2 + KCl + 4H2O
5FeCl3 + MnCl2 + KCl + 4H2O
FeS2 + O2 ![]() SO2↑ + Fe2O3
SO2↑ + Fe2O3
4FeS2 + 11O2 ![]() 8SO2↑ + 2Fe2O3
8SO2↑ + 2Fe2O3
Cu2O + H2SO4 ![]() CuSO4 + Cu + H2O + O2↑
CuSO4 + Cu + H2O + O2↑
3Cu2O + H2SO4 ![]() CuSO4 + 5Cu + H2O + O2↑
CuSO4 + 5Cu + H2O + O2↑
PbO2 + MnSO4 + HNO3 ![]() PbSO4 + HMnO4 +Pb(NO3)2 + H2O
PbSO4 + HMnO4 +Pb(NO3)2 + H2O
5PbO2 + 2MnSO4 + 6HNO3 ![]() 2PbSO4 + 2HMnO4 +3 Pb(NO3)2 + 2H2O
2PbSO4 + 2HMnO4 +3 Pb(NO3)2 + 2H2O
As2S3 + KMnO4 + H2SO4 ![]() H3AsO4 + K2SO4 + MnSO4 + H2O
H3AsO4 + K2SO4 + MnSO4 + H2O
Глассарий
- Восстановителями называют атомы, молекулы или ионы, которые отдают электроны в процессе окисления.
- Восстановление – процесс присоединения электронов.
- Окисление - процесс отдачи электронов
- Окислителями называются атомы, молекулы или ионы, которые присоединяют электроны в процессе восстановления.
- Окислительно-восстановительными реакциями называются химические реакции, которые протекают с изменением степеней окисления атомов в молекулах реагирующих веществ.
- Подкислитель – это какая – либо кислота.
- Электронные уравнения – уравнения, которые выражают процессы окисления и восстановления.
Полезные ссылки
нету
Видеоурок «Качественные реакции в химии». Сайт «Видеоуроки в интернет» (Электронный ресурс). //URL:.https://www.youtube.com/watch?v=pk7UXWVBC9U&t=193s (дата обращения 07.03.18.)
Бибилиография
- Д.Д.Дзудцова, Л.Б.Бестаева «Окислительно – восстановительные реакции». Дрофа. М. 2005 г.
- Химия .Пособие – репетитор. Ростов - на – Дону. 1997г.
- Хомченко Г. П., Севастьянова К. И., Окислительно-восстановительные реакции, 2 изд., М., 1980;
Художественная литература
- Рафаэль Сабатини «Одиссея капитана Блада» Впервые издана в 1922 году.
- Шадерло де Лакло 2Опасные связи « Наука 1965 г. «Литературные памятники»
- Фенимор Купер «Следопыт, Зверобой, Последний из могикан, Пионеры, Чингачгук» . Пенталогия Бинезун, 2014г.
- Фенимор Купер, 31 книга. Медиакнига, 2014 г.
- Анна и Серж Голон «Анжелика в Новом свете», «Дорога надежды»,» Анжелика и ее победа», «Анжелика в Квебеке», Ташкент, 1993 г.
Лев Владимирович Писаржевский (1874-1938) - выдающийся ученый в области физической химии, академик АН СССР, лауреат Премии им.Ленина.
Писаржевский создал основы электронной теории окислительно-восстановительных реакций, предложил теорию гальванического элемента, которая объяснила происхождение электродных потенциалов, создал электронную теорию катализа. В учебнике "Введение в химию" (1926 год) впервые весь материал был изложен с позиции электронной теории строения атомов и молекул.
Открыли Америку – (Новый свет) испанцы, обследовали испанцы и португальцы. Осваивали ее французы, которые отправляли туда всех своих заключенных. Французы строили форты, охотились, начали заниматься земледелием. А в Аглии правила Елизавета I, которая поощряла морской разбой, имея хороший флот. И не только поощряла пиратов, а даже давала им дворянские звания. За это они платили Англии дань из своих награбленных богатств.
Война никогда не была объявлена, но велась на море и на суше в Северной Америке. Английские пиратские суда топили французские корабли, которые везли порох или компоненты пороха, особенно калийную селитру, из Франции. Достаточно было одного ядра из пушки пиратского корабля, чтобы судно с порохом взлетело от взрыва. Во французских фортах возник острый дефицит пороха. Форты были хорошо укреплены, были солдаты, было оружие. Не было возможности выстрелить. И форты выкидывали белый флаг на милость английской армии. Захват происходил практически бескровно. Так французы потерпели поражение, а территорию Северной Америки захватили англичане.
В давние времена, когда люди не знали химии, они не могли написать уравнение реакции растворения жемчужины в виноградном уксусе:
CaCO3 + 2CH3COOH ![]() Ca(CH3COO)2 + H2O + CO2
Ca(CH3COO)2 + H2O + CO2
или даже более простой реакции сгорания алмаза на воздухе под действием солнечных лучей:
C + O2 ![]() CO2
CO2
И уж тем более никто не смог бы разъяснить, что вторая реакция намного сложнее первой: ведь при ней происходит перемещение электронов от одного атома к другому, а значит, она относится к окислительно–восстановительным реакциям. Ученые полагали, что окисление – это потеря флогистона (особого невидимого горючего вещества), а восстановление – его приобретение. Но после создания А. Лавуазье кислородной теории горения к началу XIX в. химики стали считать окислением взаимодействие веществ с кислородом, а восстановлением их превращения под действием водорода.
Но вот простейшая реакция железа с соляной кислотой:
Fe + 2HCl ![]() FeCl2 + H2↑
FeCl2 + H2↑
Здесь нет кислорода, и тем не менее железо окисляется. В этой реакции окислитель – ион водорода, а железо выступает в роли восстановителя.
Разобраться в этом удалось лишь с введением в химию электронных представлений. Теперь мы знаем, что окислитель – вещество, которое приобретает электроны, а восстановитель – вещество, которое их отдает.