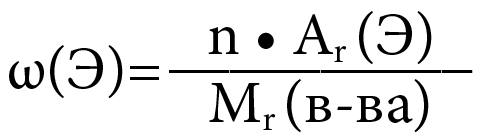Химия: Количественные соотношения — различия между версиями
Admine2 (обсуждение | вклад) (→Относительная атомная и молекулярная массы) |
Admine2 (обсуждение | вклад) (→Относительная атомная и молекулярная массы) |
||
| Строка 82: | Строка 82: | ||
Современные методы исследования позволяют определить чрезвычайно малые массы атомов с большой точностью. Так, например, '''масса атома углерода равна 1,993•10<sup>-26</sup> кг.''' Это очень маленькая величина. Поэтому в химии используются не абсолютные значения атомных масс, а относительные. За единицу атомной массы принята атомная единица массы, равная 1/12 части массы атома углерода. | Современные методы исследования позволяют определить чрезвычайно малые массы атомов с большой точностью. Так, например, '''масса атома углерода равна 1,993•10<sup>-26</sup> кг.''' Это очень маленькая величина. Поэтому в химии используются не абсолютные значения атомных масс, а относительные. За единицу атомной массы принята атомная единица массы, равная 1/12 части массы атома углерода. | ||
Относительной атомной массой химического элемента называется величина, показывающая во сколько раз масса данного атома больше 1/12 массы атома углерода. Она обозначается буквой А<sub>r</sub>. | Относительной атомной массой химического элемента называется величина, показывающая во сколько раз масса данного атома больше 1/12 массы атома углерода. Она обозначается буквой А<sub>r</sub>. | ||
| + | {{left|[[file:C-massa.png|150px|Стрелкой обозначена относительная атомная масса углерода]]}} | ||
| + | '''Относительные атомные массы указаны в периодической таблице.''' | ||
| − | |||
| − | |||
Стрелкой обозначена относительная атомная масса углерода | Стрелкой обозначена относительная атомная масса углерода | ||
Версия 08:12, 5 декабря 2017
Закон Авогадро. Молярный объём газов
Закон Авогадро: в равных объёмах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул.
(1811 г, итальянский учёный Амедео Авогадро) Лоренцо Романо Амедео Карло Авогадро ди Кваренья э ди Черрето
Cледствия закона Авогадро:
1 следствие:
Так, 6,02 ∙ 1023 молекул (1 моль) любого газа и любой смеси газов при (н.у.) занимает объём равный 22,4 л.
Такой объём называется молярным объёмом и обозначается Vm
Молярный объём – это постоянная величина для веществ – газов при нормальных условиях (н.у.): Vm = 22,4 л/моль нормальные условия – это p (давление) = 1 амт (101325 Па) t (температура) = 0 ˚C (273 К)
2 следствие:
Эта величина называется относительной плотностью D
Взаимосвязь молярной массы, молярного объёма, числа Авогадро и количества вещества: υ = V / Vm = N / Na = m / M M = ρVm
Относительная атомная и молекулярная массы
Атомы имеют очень маленький размер и очень маленькую массу. Если выражать массу атома какого-нибудь химического элемента в граммах, то это будет число перед которым находится более двадцати нулей после запятой. Поэтому измерять массу атомов в граммах неудобно.
Однако, если принять какую-либо очень малую массу за единицу, то все остальные малые массы можно выражать как отношение к этой единицы. В качестве единицы измерения массы атома была выбрана 1/12 часть массы атома углерода.
Относительной атомной массой является величина, равная отношению реальной массы атома конкретного химического элемента к 1/12 реальной массы атома углерода. Это безразмерная величина, так как делятся две массы.
Ar = mат. / (1/12)mугл.
Однако абсолютная атомная масса равна относительной по значению и имеет единицу измерения а.е.м.
То есть относительная атомная масса показывает, во сколько раз масса конкретного атома больше 1/12 атома углерода. Если у атома Ar = 12, значит его масса в 12 раз больше 1/12 массы атома углерода, или, другими словами, в нем 12 атомных единиц массы. Такое может быть только у самого углерода (C). У атома водорода (H) Ar = 1. Это значит, что его масса равна массе 1/12 части от массы атома углерода. У кислорода (O) относительная атомная масса равна 16 а.е.м. Это значит, что атом кислорода в 16 раз массивнее 1/12 атома углерода, в нем 16 атомных единиц массы.
Самый легкий элемент — это водород. Его масса примерно равна 1 а.е.м. У самых тяжелых атомов масса приближается к 300 а.е.м.
Обычно для каждого химического элемента его значение абсолютной массы атомов, выраженных через а. е. м. округляют.
Значение атомных единиц массы записаны в таблице Менделеева.
Для молекул используется понятие относительной молекулярной массы (Mr). Относительная молекулярная масса показывает, во сколько раз масса молекулы больше 1/12 массы атома углерода. Но поскольку масса молекулы равна сумме масс составляющих ее атомов, то относительную молекулярную массу можно найти, просто сложив относительные массы этих атомом. Например, в молекулу воды (H2O) входят два атома водорода с Ar = 1 и один атом кислорода с Ar = 16. Следовательно, Mr(Н2O) = 18.
Ряд веществ имеет немолекулярное строение, например металлы. В таком случае их относительную молекулярную массу считают равной их относительной атомной массе. В химии важным является величина, которая называется массовая доля химического элемента в молекуле или веществе. Она показывает, какая часть относительной молекулярной массы приходится на данный элемент. Например, в воде на водород приходится 2 доли (так как два атома), а на кислород 16. То есть, если смешать водород массой 1 кг и кислород массой 8 кг, то они прореагируют без остатка. Массовая доля водорода равна 2/18 = 1/9, а массовая доля кислорода 16/18 = 8/9.
Современные методы исследования позволяют определить чрезвычайно малые массы атомов с большой точностью. Так, например, масса атома углерода равна 1,993•10-26 кг. Это очень маленькая величина. Поэтому в химии используются не абсолютные значения атомных масс, а относительные. За единицу атомной массы принята атомная единица массы, равная 1/12 части массы атома углерода. Относительной атомной массой химического элемента называется величина, показывающая во сколько раз масса данного атома больше 1/12 массы атома углерода. Она обозначается буквой Аr.
Относительные атомные массы указаны в периодической таблице.
Стрелкой обозначена относительная атомная масса углерода
Например Аr(Н)=1, Аr(С)=12. Атомные массы округляем до целых величин, исключая атом хлора - Аr(Cl)=35,5.
Например Мr(H2SO4)=1•2+32+16•4=98.
Итак, чтобы узнать относительную молекулярную массу воды (Н2O) мы складываем относительные атомные массы с учётом индексов:
Относительная атомная масса водорода равна 1 (по таблице Менделеева) по формуле мы видим,что у нас есть 2 водорода (так как после водорода стоит индекс 2);
Относительная атомная масса кислорода равна 16 (по таблице Менделеева);
Рассчитаем относительную молекулярную массу:
Мr(Н2O)=1•2+16=16+2=18
(1•2) т.к у нас 2 водорода.
Количество вещества
Массовые отношения(массовая доля элемента)
- Формула:
-
Где:
ω(Э) – массовая доля элемента Э в веществе
n – число атомов элемента Э в веществе (индекс)
Ar – относительная атомная масса элемента Э
Mr(в-ва) – относительная молекулярная масса вещества
Качественный состав молекулы показывает какие виды атомов входят в состав вещества.
Количественный состав показывает сколько атомов определённого вида входит в состав молекулы вещества.
Закон постоянства веществ
К основным законам химии относится закон постоянства состава:
Закон постоянства состава впервые сформулировал французский ученый-химик Ж.Пруст в 1808 г.
Он писал: "От одного полюса Земли до другого соединения имеют одинаковый состав и одинаковые свойства. Никакой разницы нет между оксидом железа из Южного полушария и Северного. Малахит из Сибири имеет тот же состав, как и малахит из Испании. Во всем мире есть лишь одна киноварь".
В этой формулировке закона, как и в приведенной выше, подчеркивается постоянство состава соединения независимо от способа получения и места нахождения.
Чтобы получить сульфид железа(II), мы смешивали железо и серу в соотношении 7:4. Посмотрите видео-эксперимент. Если смешать их в другой пропорции, например 10:4, то химическая реакция произойдет, но 3 г железа в реакцию не вступит. Почему наблюдается такая закономерность? Известно, что в сульфиде железа(II) на каждый один атом железа приходится один атом серы. Следовательно, для реакции нужно брать вещества в таких массовых соотношениях, чтобы сохранялось соотношение атомов железа и серы (1:1). Поскольку численные значения атомных масс Fe, S и их относительных атомных масс Ar(Fe), Ar(S) совпадают, можно записать:Ar(Fe):Ar(S) = 56:32 = 7:4.
Отношение 7:4 сохраняется постоянно, в каких бы единицах массы ни выражать массу веществ (г, кг, т, а.е.м.). Большинство химических веществ обладает постоянным составом.
(демонстрация кристаллической решетки, рис.)
Рис. Кристаллическая решетка сульфида железа(II)
Развитие химии показало, что наряду с соединениями постоянного состава существуют соединения переменного состава. По предложению Н.С. Курнакова первые названы дальтонидами (в память английского химика и физика Дальтона), вторые - бертоллидами(в память французского химика Бертолле, предвидевшего такие соединения). Состав дальтонидов выражается простыми формулами с целочисленными стехиометрическими индексами, например Н2О, НCl, ССl4, СO2. Состав бертоллидов изменяется и не отвечает стехиометрическим отношениям.
В связи с наличием соединений переменного состава в современную формулировку закона постоянства состава следует внести уточнение.
Cостав соединений молекулярной структуры, т.е. состоящих из молекул, - является постоянным независимо от способа получения. Состав же соединений с немолекулярной структурой (с атомной, ионной и металлической решеткой) не является постоянным и зависит от условий получения.
На основе закона постоянства состава можно производить различные расчёты, например:
В каких массовых отношениях соединяются химические элементы в серной кислоте, химическая формула которой H2SO4?
Решение: Используя ПСХЭ найдём относительные атомные массы химических элементов: Ar(H)=1, Ar(S)=32, Ar(O)=16.
Определим массовые отношения этих элементов в формуле H2SO4 m(H) : m(S) : m(O) = 2Ar(H) : Ar(S) : 4Ar(O) = 2 : 32 : 64 = 1 : 16 : 32
Таким образом, чтобы получить 49 г серной кислоты (1+16+32=49), необходимо взять 1 г - Н, 16 г - S и 32 г - О.
Закон сохранения массы веществ
Проблемный вопрос: изменится ли масса реагирующих веществ по сравнению с массой продуктов реакции?
Чтобы ответить на данный вопрос понаблюдайте за следующим экспериментом
Видео-эксперимент: Нагревание меди.
Описание эксперимента: В коническую колбу помесите 2 грамма измельченной меди. Плотно закройте колбу пробкой и взвесьте. Запомните массу колбы. Осторожно нагревайте колбу в течение 5 минут и наблюдайте за происходящими изменениями. Прекратите нагревание, и когда колба охладится, взвесьте её. Сравните массу колбы до нагревания с массой колбы после нагревания. Вывод: Масса колбы после нагревания не изменилась.
Понаблюдаем за другими видео-экспериментами:
Горение свечи в замкнутом сосуде
Сохранение массы веществ в реакциях
Вывод: Масса веществ до и после реакции не изменилась.
Формулировка закона сохранения массы: масса веществ, вступивших в реакцию, равна массе образовавшихся веществ.
Закон сохранения массы веществ является основным законом химии, все расчеты по химическим реакциям производятся на его основе. Именно с открытием этого закона связывают возникновение современной химии как точной науки.
Закон сохранения массы был теоретически открыт в 1748 году и экспериментально подтверждён в 1756 году русским ученым М.В. Ломоносовым.
Французский учёный Антуан Лавуазье в 1789 году окончательно убедил учёный мир в универсальности этого закона. Как Ломоносов, так и Лавуазье пользовались в своих экспериментах очень точными весами. Они нагревали металлы (свинец, олово, и ртуть) в запаянных сосудах и взвешивали исходные вещества и продукты реакции.
Химические уравнения
Закон сохранения массы веществ применяется при составлении уравнений химических реакций.
Химическое уравнение – это условная запись химической реакции посредством химических формул и коэффициентов.
Посмотрим видео - эксперимент: Нагревание смеси железа и серы.
В результате химического взаимодействия серы и железа получено вещество – сульфид железа (II) – оно отличается от исходной смеси. Ни железо, ни сера не могут быть визуально обнаружены в нем. Невозможно их разделить и с помощью магнита. Произошло химическое превращение.
Новые вещества, образующиеся в результате химической реакции называются продуктами.
Запишем протекающую реакцию в виде уравнения химической реакции:
Fe + S = FeS
Алгоритм составления уравнения химической реакции
Составим уравнение химической реакции взаимодействия фосфора и кислорода 1. В левой части уравнения записываем химические формулы реагентов (веществ, вступающих в реакцию). Помните! Молекулы большинства простых газообразных веществ двухатомны – H2; N2; O2; F2; Cl2; Br2; I2. Между реагентами ставим знак «+», а затем стрелку:
P + O2
2. В правой части (после стрелки) пишем химическую формулу продукта (вещества, образующегося при взаимодействии). Помните! Химические формулы необходимо составлять, используя валентности атомов химических элементов:
P + O2P2O5
3. Согласно закону сохранения массы веществ число атомов до и после реакции должно быть одинаковым. Это достигается путём расстановки коэффициентов перед химическими формулами реагентов и продуктов химической реакции.
Вначале уравнивают число атомов, которых в реагирующих веществах (продуктах) содержится больше.
В данном случае это атомы кислорода.
Находим наименьшее общее кратное чисел атомов кислорода в левой и правой частях уравнения. Наименьшее кратное для атомов кислорода –10:
Находим коэффициенты путём деления наименьшего кратного на число атомов данного вида, полученные цифры ставим в уравнение реакции:
P + 5O22P2O5
Закон сохранения массы вещества не выполнен, так как число атомов фосфора в реагентах и продуктах реакции не равно, поступаем аналогично ситуации с кислородом:
Получаем окончательный вид уравнения химической реакции. Стрелку заменяем на знак равенства. Закон сохранения массы вещества выполнен:
4P + 5O22P2O5
Глоссарий
- Химическое вещество характеризуется атомной массой, а молекулы — молекулярной массой.
- Атомная единица массы (а.е.м.) - ровно 1/12 часть массы атома углерода–12, в ядре которого 6 протонов и 6 нейтронов, а в электронной оболочке 6 электронов. Другое название - углеродная единица. Единица, в которой измеряют массу атомов, молекул и субатомных частиц. См. также ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА и АТОМНЫЙ ВЕС.
- Относительная атомная масса - обозначается символом Ar ("r" - от английского "relative" - относительный) - отношение массы атома к массе 1/12 атома углерода–12 (см. а.е.м.). В современной научной литературе наряду с термином относительная атомная масса используюется термин АТОМНЫЙ ВЕС (как синонимы).
- Относительная молекулярная масса (Mr) — величина, показывающая, во сколько раз масса молекулы данного вещества больше 1 / 12 массы атома углерода–12. Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов, составляющих химическое соединение, с учетом индексов.
- Моль вещества (n) — это количество вещества, содержащее столько молекул, атомов, ионов, электронов или других структурных единиц, сколько содержится их в 12 г изотопа углерода 12C.
- Число структурных единиц, содержащихся в 1 моле вещества равно 6,02 • 1023. Это число называется числом Авогадро (NA)
- Молярная масса (M) показывает массу 1 моля вещества и равна отношению массы вещества к соответствующему количеству вещества.
M = m / n
- В 1808 Ж. Пруст сформулировал Закон постоянства состава, который гласит, что независимо от способа получения все индивидуальные вещества имеют постоянный количественный и качественный состав.
- Важную роль в развитии химической науки сыграли газовые законы (справедливы только для газов).
В 1811 г. Авогадро ди Кваренья (Закон Авогадро) доказал, что - в равных объемах любых газов при постоянных условиях (температуре и давлении) содержится одинаковое число молекул. В одинаковых условиях одно и то же число молекул занимают равные объемы, а 1 моль любого газа при температуре 273 oК и давлении 101,3 кПа газа занимает объем 22,4 л, который называется молярным объемом газа (Vm).
В 1756 г. М.В. Ломоносов, после длительных испытаний, пришел к важному открытию: вес всех веществ, вступающих в химическую реакцию, равен весу всех продуктов реакции. - Закон сохранения вещества отражается в законе сохранения массы, который заключается в следующем: масса веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции. Вещества не исчезают и не возникают из ничего, а происходит химическое превращение. Закон является основой при составлении химических реакций и количественных расчетов в химии.
- Моль - количество вещества, равное 6,022 . 1023 структурных единиц данного вещества: молекул (если вещество состоит из молекул), атомов (если это атомарное вещество), ионов (если вещество является ионным соединением). Число 6,022 . 10 23 называется постоянной Авогадро или числом Авогадро.
- Молярная масса - масса одного моля вещества в граммах называется молярной массой вещества или грамм-молем (размерность г/моль). Численное выражение молярной массы (грамм-моля) в граммах совпадает с молекулярным весом (или атомным, если вещество состоит из атомов) в единицах а.е.м.
Нормальными условиями (н.у.) называют температуру 0 оС (273 K) и давление 1 атм (760 мм ртутного столба или 101 325 Па). Не путать со СТАНДАРТНЫМИ СЛОВИЯМИ! - Относительная атомная масса - обозначается символом Ar ("r" - от английского "relative" - относительный) - отношение массы атома к массе 1/12 атома углерода-12 (см. а.е.м.). В современной научной литературе наряду с термином "относительная атомная масса" используюется термин АТОМНЫЙ ВЕС (как синонимы).
- Постоянная Авогадро - 6,022 · 1023 (см. “моль”).
- Число Авогадро - 6,022 · 1023 (см. “моль”).
Полезные ссылки
Бибилиография:
НЕТУ
- Ахметов Н. С. Актуальные вопроса курса неорганической химии. — М.: Просвещение, 1991. — 224 с — ISBN 5-09-002630-0
Задача 1. Какой объем (н.у.) занимает 5·10-3 кг углекислого газа?
Найдем молекулярную массу СО2:
Mr(CO2)= 12+2·16=44 г.
Tакже нам известен молярный объем газа, который равен 22,4 м3.
Составим следующую пропорцию:
44 кг СО2 занимает объем 22,4 м3
5·10-3 кг СО2 занимает объем – х
откуда х=(5·10-3·22,4)/44=2,5·10-3 м3
Таким образом, 5·10-3 кг углекислого газа занимает объем равный 2,5·10-3 м3.
Задача 2. Определить массу 0,9·10-3 м3 кислорода при 21 °С и давлении 96000 Па, если масса 10-3 м3 кислорода равна 1,5·10-3 кг при нормальных условиях.
Найдем температуру в Кельвинах Т=273+21=294 К;
Найдем объем газа, приведенный к н.у. по формуле
P1V1 / T1 = P2V2 / T2;
V1= T1P2V2 / T2P1=
=(273·96000·0.9·10-3) / (294·101325)=0.8·10-3 м3
Теперь рассчитаем массу вычисленного объема:
10-3 м3 кислорода имеют массу равную 1,5·10-3 кг
0,8·10-3 м3 кислорода имеют массу равную х
х = 0,8·10-3·1,5·10-3/10-3=1,2·10-3 кг
Таким образом, 0,8·10-3 м3 кислорода имеют массу равную 1,2·10-3 кг.
Задача 3. Рассчитайте объем атома железа, если его плотность равна 7900 кг/м3
Найдем молярный объем железа (M(Fe)=56 г.)
V=n/ρ=56/7900=7,1·10-3 м3
Условно примем, что атомы имеют форму шара и в кристалле касаются друг друга, то истинный объем будет составлять только 74% от общего объема:
V=0,071·0,74=5,25·10-3 м3
Тогда объем одно атома железа будет равен:
VА=5,25·10-3/6,02·1026=8,7·10-30 м3
Задача 4. Определить массу молекулы газа, если масса 10-3 м3 газа, при н.у., равна 0,3810-3 кг.
Число молекул 1 кмоль любого вещества равна числу Авогадро (6,02·1026 ), поэтому для начала определим 1 кмоль газа:
10-3 м3 газа имеют массу равную 0,3810-3 кг
22,4 м3 газа имеют массу равную — х
х=22,4·0,3810-3/10-3=7,6 кг,
Далее определяем массу молекулы газа:
m=7,6/6,02·1026=1,26·10-26 кг.
Задача 5. Рассчитайте молярную массу эквивалента металла, если при соединении 7,2 г. металла с хлором было получено 28,2 г. соли. Молярная масса эквивалента хлора равна 35,45 г/моль
Согласно закону эквивалента отношение массы металла и соли должно быть равно отношению их молярных масс эквивалентов. Обозначим молярную массу эквивалента металла через х, тогда:
7,2/28,2=х/(х+35,45)
Решая уравнение, находим, что х=12,15 г/моль.
Таким образом, молярная масса эквивалента металла Мэкв=12,15 г/моль.
Задача 6. Определение молярной массы эквивалента сложных веществ в реакциях обмена
Определите молярные массы эквивалентов H2SO4 в следующих реакциях:
А) H2SO4+2KOH = K2SO4+2H2O
Б) H2SO4+KOH = KHSO4+H2O
Значение эквивалента вещества зависит от того, в какой именно реакции оно участвует.
В реакции А) 1 моль H2SO4 взаимодействует с 2 моль KOH, а эквивалент H2SO4 с 2 эквивалентами KOH. Молярная масса эквивалента KOH равна его молекулярной массе, следовательно, молярная масса эквивалента H2SO4 равна половине ее молекулярной массы:
Мэкв=98/2=49 г/моль
В реакции Б) 1 моль H2SO4 взаимодействует с 1 моль KOH, а эквивалент H2SO4 с 1 эквивалентами KOH. Молярная масса эквивалента KOH равна его молекулярной массе, следовательно, молярная масса эквивалента H2SO4 равна ее молекулярной массе: 98 г/моль.
Задача 7. Рассчитайте молярную массу эквивалента кислоты, если на нейтрализацию 9 г. ее израсходовано 8 г. гидроксида натрия.
Молярная масса эквивалента гидроксида натрия равна его молекулярной массе Мэкв =40 г/моль.
Вещества взаимодействуют между собой в массах, пропорциональных из молярным массам эквивалента, т.е.:
Обозначим молярную массу эквивалента кислоты – х, тогда
9/8=х/40=45 г/моль
Задача 8. Найдите молекулярную формулу вещества, если относительная плотность паров этого вещества по водороду равна 67,5, а массовые доли элементов (%) в веществе следующие: серы – 23,7, кислорода – 23,7, хлора – 52.
Формулу искомого соединения можно представить как SxOyClz. Найдем соотношение между числом атомов S, O, Cl делением его содержания на его атомную массу:
x:y:z = 23,7/32 : 23,7/16 : 52/35,5 = 0,74 : 1,48 : 1,46
Делим все полученные соотношения на наименьшее, получаем:
x:y:z =1:2:2
Простейшая формула вещества SO2Cl2
Его молекулярная масса равна Mr = 32+16·2+35,5·2 = 135 г.
Теперь найдем молекулярную массу вещества по плотности паров этого вещества по водороду:
Mr = 2DH2= 2·67,5 = 135 г.
Следовательно, истинная формула вещества совпадает с простейшей: SO2Cl2
Задача 9. Рассчитайте молекулярную массу газа, если 7·10-3 кг. его при 20°С и 0,253·105 Па занимают объем 22,18·10-3 м3
В данном случае, вычислить молярную массу газа можно, используя уравнение Клапейрона – Менделеева:
pV = nRT = (m/M)RT;
R=8,3144·103 Дж/моль·К
Т=273+20=293 К
М=mRT/pV=7·10-3·8,3144·103293/(0,253·105·22,18·10-3)=30,35 г/моль
Молярная масса газа равна 30,35 г/моль
Задача 10. При 0°С в сосуде объемом 14·10-3 м3 содержится 0,8·10-3 кг водорода и 6,3·10-3 кг азота. Определите парциальное давление азота и общее давление смеси.
Найдем количества вещества водорода и азота:
n=m/Mn(H2)=0,8·10-3/2=0,4·10-3моль
n(N2)= 6,3·10-3/28=0,225·10-3моль
Далее, с помощью уравнения Клапейрона – Менделеева, найдем парциальное давление каждого газа в смеси:
pV = nRT = (m/M)RT;
p = nRT/V;
p(H2)=n(H2)
RT/V=0,4·10-3·8,3144·103·273/14·10-3=64,85·103Па
p(N2)= n(N2)
RT/V=0,225·10-3*8,3144·103·273/14·10-3=36,479·103Па
pобщ=p(H2)+p(N2)= 64,85·103+36,479·103=101329 Па
Задача 11. Газовая смесь составлена из 5·10-3 м3 метана под давлением 96000 Па, 2·10-3 м3 водорода под давлением 84000 Па и 3·10-3 м3 диоксида углерода под давлением 109000 Па. Объем смеси 8·10-3 м3. Определите парциальные давления газов в смеси и общее давление смеси.
Сначала найдем парциальное давление каждого из газов:
p(CH4)=P(CH4)·V(CH4)/Vобщ=96000·5·10-3/8·10-3=60000 Па
p(H2)=P(H2)·V(H2)/Vобщ=84000·2·10-3/8·10-3=21000 Па
p(CО2)=P(CО2)·V(CО2)/Vобщ=109000·3·10-3/8·10-3=40875 Па
Общее давление:
pобщ= p(CH4)+ p(H2)+ p(CО2)= 60000+21000+40875=121875 Па
Задача 12.Газовая смесь состоит из оксида и диоксида азота. Вычислите парциальные давления газов в смеси, если объемные доли газов соответственно равны (%) 37,5 и 62,5. Общее давление газовой смеси 106640 Па.
Парциальное давление газа в смеси равно произведению общего давления на его объемную долю в смеси:
p(NO)= pобщ·φNO=106640·0,375=39990 Па
p(NO2)= pобщ·φNO2=106640·0,625=66650 Па
Дочитаем всю страницу…
Имена координат
Даст отгадка двух шарад.
I.
Три буквы плода треугольного,
Две буквы от стола, от школьного,
"П" между этими фрагментами…
Все вместе - столбик с элементами!
Группа
II.
Птичий мех, но не пух, и без букв последних двух,
Плюс раствор для смазки ссадин, что сажают дети за день;
Вместе - ряд горизонтальный получаем моментально.
Период
Предупреждаю вас заранее:
Я непригоден для дыхания!
Но все как будто бы не слышат
И постоянно мною дышат.
yt
...
Я светоносный элемент.
Я спичку вам зажгу в момент.
Сожгут меня - и под водой
Оксид мой станет кислотой.
Фосфор?
...
У меня дурная слава:
Я - известная отрава.
Даже имя говорит,
Что я страшно ядовит.
yt